Відмінності між версіями «Сербина М.П.»
Матеріал з Київський столичний університет імені Бориса Грінченки
(→Хімічний зв"язок) |
(→Обчислення за хімічними формулами) |
||
| Рядок 32: | Рядок 32: | ||
===ІІ семестр=== | ===ІІ семестр=== | ||
====Обчислення за хімічними формулами==== | ====Обчислення за хімічними формулами==== | ||
| + | Кількість речовини | ||
| + | <br> | ||
| + | Молярна маса | ||
| + | <br> | ||
| + | Закон Авогадро. Об"єм молярний | ||
| + | <br> | ||
| + | Відносна густина газу. | ||
| + | |||
===Основні класи неорганічних сполук=== | ===Основні класи неорганічних сполук=== | ||
=====Оксиди, кислоти===== | =====Оксиди, кислоти===== | ||
Версія за 17:42, 23 січня 2021
Зміст
Хімія 8 клас
І семестр
ПС хімічних елементів Д.І. Менделєєва
Короткі відомості про способи класифікації хімічних елементів. Поняття про лужні, інертні елементи, галогени/
Періодичний закон Д.І. Менделєєва. Періодична система хімічних елементів, її структура.
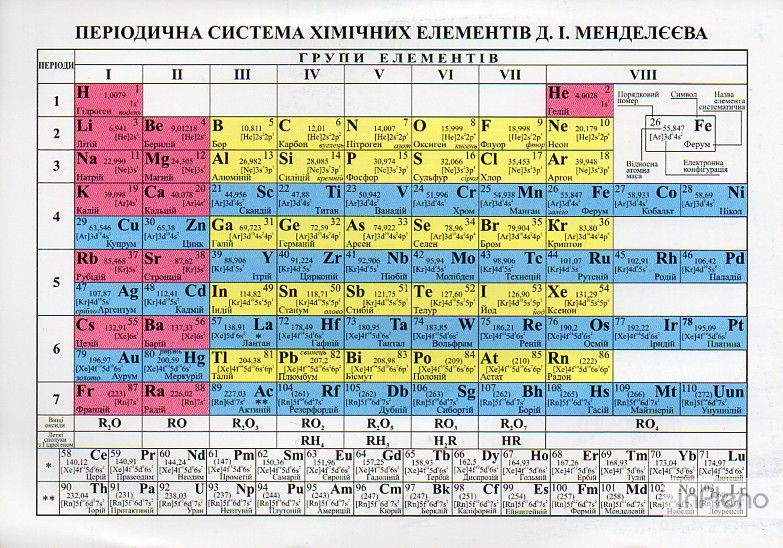
Будова атома. Склад атомних ядер (протони і нейтрони). Протонне число. Нуклонне число. Сучасне формулювання періодичного закону.
Стан електронів в атомі. Електронні орбіталі. Енергетичні рівні та підрівні, їхнє заповнення електронами хімічних елементів. Будова електронних оболонок атомів хімічних елементів №1 - 20
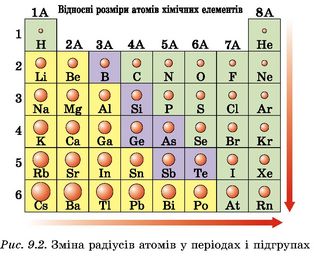
Поняття про радіус атома.
Періодична система хімічних елементів з позиції теорії позиції будови атома.
Характеристика хімічних елементів за їхнім місце у періодичній системі
Хімічний зв"язок
Природа хімічного зв"язку. Електронегативність.
Ковалентний зв"язок. Утворення ковалентного неполярного зв"язку.
Ковалентний зв"язок. Утворення ковалентного полярного зв"язку.
Йони. Йонний зв"язок, його утворення.
ІІ семестр
Обчислення за хімічними формулами
Кількість речовини
Молярна маса
Закон Авогадро. Об"єм молярний
Відносна густина газу.